R. Menè, C. Torlasco. G. Parati
Scuola di Specializzazione in Malattie dell’Apparato Cardiovascolare, Milano Bicocca
ABSTRACT
Un paziente di 77 anni viene ricoverato per accertamenti in seguito a riscontro di frequenti episodi di tachicardia ventricolare non sostenuta (TVNS). In anamnesi riporta ipertensione arteriosa, diabete mellito e sarcoidosi polmonare in remissione da più di dieci anni. Alla telemetria (TLM) vengono registrate frequenti TVNS a più morfologie. La risonanza magnetica (RM) cardiaca evidenzia presenza di late gadolinium enhancement (LGE) infero-postero-laterale e settale con edema alle sequenze di mapping. Dato l’alto sospetto clinico viene iniziata la terapia per sarcoidosi cardiaca con cortisone ad alte dosi e beta bloccante, ottenendo una drastica riduzione del burden aritmico. La tomografia ad emissione di positroni (PET) cardiaca, tuttavia, risulta essere negativa. Vengono discusse due possibili spiegazioni della discrepanza fra reperti RM e PET in corso di sarcoidosi cardiaca.
CASO CLINICO
Un paziente di 77 anni giungeva in ambulatorio portando in visione il monitoraggio elettrocardiografico di 24 ore secondo Holter, eseguito per episodi pre-sincopali, che evidenziava fasi di blocchi atrio-ventricolari (BAV) di secondo grado tipo Mobitz I, frequentissimi battiti extrasistolici ventricolari (BEV) e numerose salve di TVNS. Il paziente riferiva l’esecuzione di un Holter ECG due anni prima, portato in visione all’equipe medica, che evidenziava rare salve di TVNS, per cui aveva avviato la terapia con amiodarone, in assenza di beneficio clinico. In tale occasione tra gli accertamenti aveva eseguito uno studio coronarografico, risultato negativo. In anamnesi riportava ipertensione arteriosa, in terapia con diuretico e calcio antagonista, e diabete mellito tipo 2 in terapia con ipoglicemizzante orale. All’età di 50 anni aveva ricevuto una diagnosi istologica di sarcoidosi polmonare trattata con terapia steroidea e da allora in remissione.
In considerazione della sintomaticità e della frequenza degli eventi aritmici ventricolari il paziente veniva ricoverato per ulteriori accertamenti.
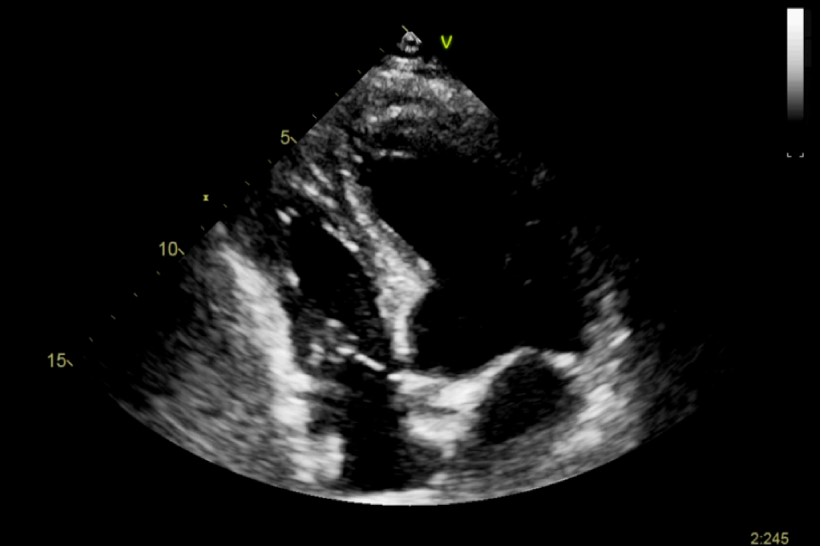
Obiettivamente all’ingresso il paziente era in buon compenso cardiocircolatorio. L’ECG a 12 derivazioni mostrava un ritmo sinusale normofrequente condotto con BAV I, blocco di branca destra (BBDx) ed emiblocco anteriore sinistro (EAS). Eseguiva quindi ecocardiogramma transtoracico che rilevava un assottigliamento del setto interventricolare (Figura 1) prossimale con movimento asincrono setto-apicale, frazione d’eiezione (FE) del 55%, pressione polmonare arteriosa sistolica (PAPs) 40-50 mmHg e insufficienza mitralica e tricuspidale di grado moderato.
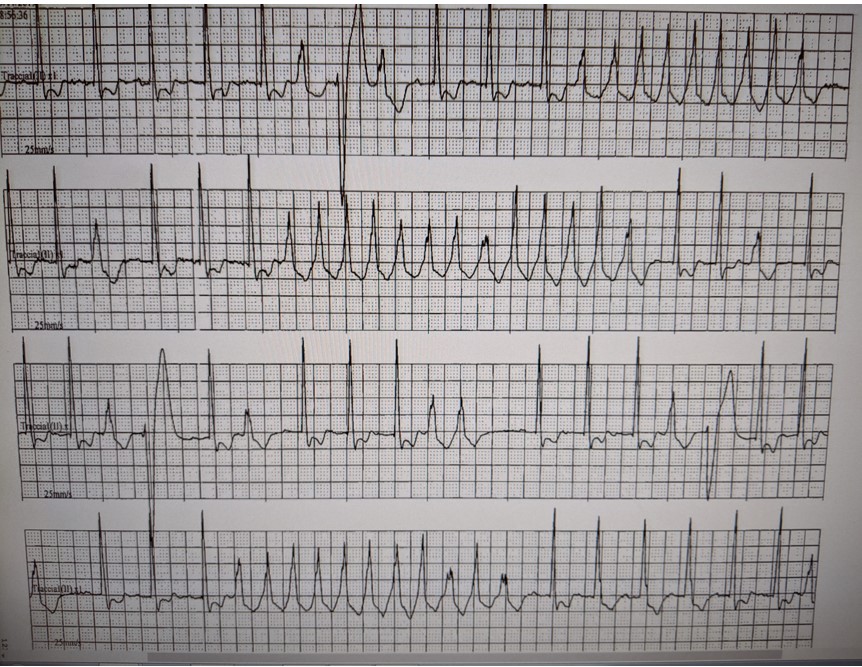
Alla telemetria ECG vengono rilevate frequenti salve di TVNS con morfologia variabile (Figura 2).
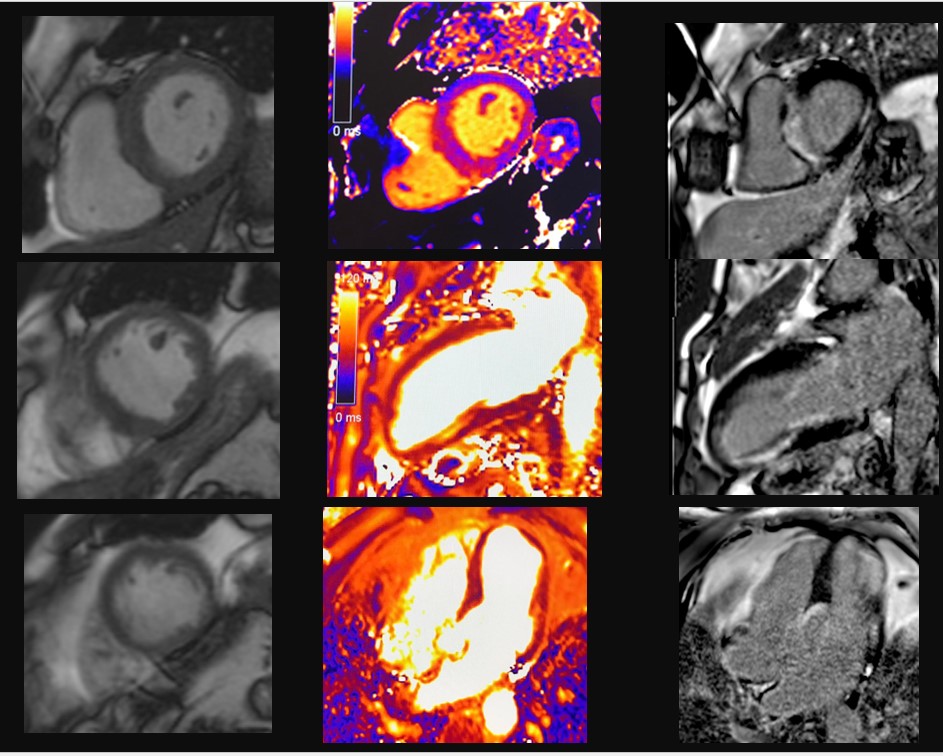
Veniva quindi eseguita, durante il ricovero, la RM cardiaca che rilevava edema della parete infero-postero-laterale medio-distale e del setto in toto, nelle sequenze T1 e T2 mapping, e LGE con pattern intramiocardico (non ischemico) nelle medesime regioni (Figura 3).
In considerazione dell’elevato sospetto clinico di coinvolgimento cardiaco di sarcoidosi sistemica, veniva iniziata terapia con cortisone ad alte dosi (prednisone 37,5 mg) e betabloccante (carvedilolo 6,25 mg x 2). Il paziente veniva inoltre sottoposto a impianto di un defibrillatore impiantabile (ICD) bicamerale.
Per confermare la diagnosi, il paziente veniva inviato ad eseguire una PET con 18F-FDG che, tuttavia, risultava negativa per uptake patologico nel tessuto miocardico.
Nonostante l’esito inaspettatamente negativo della PET, veniva proseguita la terapia farmacologica già impostata. A 48 ore dall’inizio della terapia si assisteva ad una drastica riduzione del burden aritmico alla telemetria, per cui il paziente veniva dimesso al domicilio. Alla visita di follow-up dopo 3 mesi il paziente riferiva un ottimo controllo dei sintomi e nessuna scarica dell’ICD è stata registrata.
DISCUSSIONE
Abbiamo presentato un caso di sarcoidosi cardiaca con una inusuale discrepanza fra reperti RM e PET.
La sarcoidosi cardiaca si manifesta nel 5-25% dei pazienti affetti da sarcoidosi con blocchi di conduzione, aritmie ventricolari e scompenso cardiaco. La diagnosi viene posta in seguito a conferma istologico o, più frequentemente, secondo dei criteri diagnostici basati sulla compresenza di: 1) conferma istologica di sarcoidosi extracardiaca; 2) almeno uno fra cardiomiopatia responsiva a terapia steroidea, FE<40% altrimenti inspiegata, presenza di TV altrimenti inspiegate, BAV II Mobitz II o BAV III, uptake patologico alla PET, LGE alla RM cardiaca, uptake patologico di gallio; 3) assenza di altre cause che spieghino le manifestazioni cardiache del paziente (1).
I due esami di imaging più frequentemente utilizzati sono la PET e la RM cardiaca. Ciascuno di questi esami ha una accuratezza riportata del 75-90% e, secondo i criteri diagnostici, possono essere usati alternativamente per confermare la diagnosi di sarcoidosi cardiaca.
Una prima ipotesi avanzata per giustificare la discrepanza fra reperti RM e PET è stata una possibile inadeguata preparazione all’esame di PET cardiaca. E’ infatti noto come il metabolismo miocardico sia glucidico esclusivamente in presenza di insulina e, in assenza di questo ormone sia basato sul metabolismo degli acidi grassi. L’obiettivo della preparazione è quindi di abbattere i livelli di insulina tramite una dieta ricca in acidi grassi e povera in glucosio nelle 48 ore precedenti all’esame (oltre all’astinenza dall’esercizio fisico e dalla somministrazione di insulina). Un’inadeguata osservanza di questa preparazione porta quindi il paziente ad eseguire l’esame con l’intero miocardio, e non solo con l’infiltrato cellulare patologico, dipendente dal metabolismo glucidico e quindi captante 18-FDG. L’assenza di un gradiente di captazione fra miocardio sano ed infiltrato determina quindi una considerevole riduzione della sensibilità dell’esame. Tuttavia, nel nostro caso, tutti i criteri di preparazione sono stati osservati.
Un’ulteriore ipotesi, che è stata avanzata, si basa sulle differenti alterazioni istologiche che i due esami sono in grado di evidenziare: nella RM il gadolinio tende ad accumularsi nella matrice extracellulare, che risulta essere aumentata sia in caso di infiltrato edematoso (fase acuta della malattia) che fibroso (esiti della malattia). La distinzione fra le due fasi viene poi effettuata tramite ulteriori sequenze, quali le T1 e T2 mapping, che sono specifiche nel riconoscere l’edema. D’altro canto, nella PET il 18-FDG viene captato specificamente dall’infiltrato cellulare, tipico della fase acuta della malattia. Si può quindi ipotizzare che il nostro paziente avesse un infiltrato flogistico di fase acuta prevalentemente edematoso, per cui LGE evidenziato dall’indagine RM, e viceversa con scarsa componente cellulare, per cui PET negativo. Questa ipotesi, che ad oggi non trova riscontro in letteratura, potrebbe essere spunto per futuri studi volti a individuare differenze nella sensibilità di RM e PET cardiaca nel riconoscere la fase acuta della sarcoidosi cardiaca.
BIBLIOGRAFIA
- Birnie DH, Nery PB, Ha AC, Beanlands RS. Cardiac Sarcoidosis. J Am Coll Cardiol. 2016 Jul 26;68(4):411-21. doi: 10.1016/j.jacc.2016.03.605. PMID: 27443438.